目的 探讨骨桥蛋白(OPN)对人Tenon’s囊成纤维细胞(HTFs)的调控作用。方法 实验研究。采用不同浓度(0、0.05、0.5、5 µmol/L)的OPN对HTFs进行处理,采用MTT法检测HTFs的增殖速度,采用细胞划痕实验检测HTFs的移行速度。实时荧光定量PCR(Real-time PCR)检测不同浓度的OPN处理后HTFs的血管内皮生长因子(VEGF)和转化生长因子β(TGF-β)的mRNA水平变化。采用Western blot检测不同浓度的OPN处理后HTFs的I 型胶原蛋白的表达。采用单因素方差分析对数据进行比较。结果 不同浓度OPN处理组HTFs增殖能力和移行速度差异有统计学意义(F=174.5、297.1,P<0.01)。OPN处理组的HTFs增殖能力增强,移行速度加快,而且随着OPN的浓度增加而增加。给予OPN单克隆抗体1A12(5 µmol/L OPN+20 µg/ml 1A12)处理后HTFs增殖和移行速度变慢。不同浓度的OPN处理后HTFs中VEGF和TGF-β的mRNA含量变化差异无统计学意义。OPN处理后HTFs中I型胶原蛋白的蛋白表达增加,呈浓度依赖性(F=30.2,P<0.01)。结论 OPN能促进HTFs增殖和移行,呈浓度依赖性,该效应可被OPN抗体1A12抑制。上调OPN可以诱导HTFs中I型胶原蛋白的表达,其单克隆抗体1A12能抑制这种效应。
Objective: To assess the modulating function of osteopontin (OPN) on human Tenon’s fibroblasts (HTFs). Methods: With the intervention of OPN in different concentrations (0, 0.05 μmol/L, 0.5 μmol/L, and 5 μmol/L), the proliferation rate of HTFs was measured by 3-(4,5-dimethylthiazol-2-Yl)-2,5-diphenyltetrazolium bromide (MTT), and the motility was surveyed by the cell scratch method. Real-time polymerase chain reaction (PCR) was applied to measure the mRNA of vascular endothelial growth factor (VEGF) and transforming growth factor β (TGF-β) in HTFs in the presence of different concentration of OPN. Western blot was used to measure the collagen-I levels. Data were analyzed using ANOVA. Results: OPN induced the proliferation of HTFs as indicated by MTT and enhanced the motility of HTFs as shown by the cell scratch method. The effects were concentration dependent (F=174.5, 297.1, P<0.01). In the presence of anti-OPN 1A12 (5 µmol/L OPN+20 µg/ml 1A12), the effects of OPN on HTFs were inhibited. None of the concentrations of OPN affected mRNA levels of VEGF and TGF-β mRNA. OPN augmented HTF expression of collagen-I protein in a concentration-dependent manner (F=30.2, P<0.01). Conclusions: The enhancement of HTF proliferation, motility, and collagen-I expression OPN was concentration dependent. Incubation with the monoclonal OPN antibody 1A12 inhibited the effects of OPN on the HTFs.
骨桥蛋白(Osteopontin, OPN)是一种分布于细胞外基质中的、功能复杂的磷酸化糖蛋白, 在细胞迁移、血管发生、免疫应答、肿瘤转移、炎症反应、组织重塑等多种生理和病理过程中发挥重要作用[1, 2, 3, 4]。既往的研究已经证实, OPN能够促进成纤维细胞增殖、移行, 在组织纤维化过程中发挥重要作用[2, 5, 6]。人Tenon’s囊成纤维细胞(Human Tenon’s fibroblasts, HTFs)是机体内成纤维细胞的一种, 通过增殖、迁移以及合成细胞外基质等行为在青光眼滤过手术瘢痕形成过程中发挥重要作用[7]。OPN对HTFs的影响作用尚不清楚。我们拟观察OPN及其单克隆抗体1A12对HTFs细胞增殖和移行的影响及其作用机制。
人胚眼Tenon’s囊成纤维细胞购于中国医学科学院基础医学研究所细胞中心, 实验所用的细胞为传代6~10代的细胞。鼠抗人OPN单克隆抗体1A12由第二军医大学肿瘤研究所制备。PCR所用试剂:无RNA酶的异丙醇、氯仿(美国Sigma公司), DEPC水(上海生工生物工程有限公司), TRIzol试剂(U.S.Patent No. 5β 346β 994, 美国Invitrogen公司), Rever Tra Ace反转录试剂盒(code:FSK-100, 日本TOYOBO公司), SYBR Green Realtime PCR Master Mix(code:QPK-201, 日本TOYOBO公司)。Western blot所用试剂:Bradford蛋白定量试剂(Bio-Rad Protein Assay Kit), Western blot显色试剂盒(Super signal显色试剂盒, 美国Themo Fisher公司)。抗I型Collagen兔单克隆抗体购于英国Abcam公司。Tubulin兔单克隆抗体购于美国Cell Signaling公司。Anti-mouse HRP和Anti-rabbit HRP购于美国Cell Signaling公司。
将处于对数生长期的人胚眼Tenon’s囊成纤维细胞消化计数后接种于96孔板(1β 000个/孔), 分为对照组(正常培养基)、OPN处理组(0.05、0.5、5 µ mol/L)、OPN和1A12同时处理组(5 µ mol/LOPN+20 µ g/ml 1A12), 设调零孔, 每组每种细胞均铺3复孔, 铺板24 h后, 换用含1%FBS的DMEM培养基饥饿培养12 h, 处理组按照规定的浓度加入OPN及1A12进行刺激, 而对照组加入含1%FBS的高糖培养基, 于刺激0、1、2、3、4 d后分别每孔加入Solution 1溶液10 µ l, 37 ℃孵育4 h后再加入Solution 2, 37 ℃孵育过夜, 用酶标仪检测560 nm处的吸光度(OD)值。按照下列的公式计算每种细胞经过刺激后的增长率:细胞增长率=OD值(n d)/OD值(0 d)× 100%。样本量5个, 每一样本重复3次。
取处于对数生长期的人胚眼Tenon’s囊成纤维细胞消化计数后接种于12孔板(1× 106个/孔), 分为对照组(正常培养基组)、OPN处理组(0.05、0.5、5 µ mol/L)、OPN和1A12同时处理组(5 µ mol/L OPN+ 20 µ g/ml 1A12), 铺板24 h后, 更换采用含1%FBS的DMEM培养基饥饿培养12 h, 处理组按照规定的浓度加入OPN及1A12进行刺激, 而对照组加入含1%FBS的高糖培养基。用无菌的200 µ l的Tip头造成条形细胞缺损区, PBS漂洗3次去除悬浮细胞, 于0、12、24 h时在倒置相差显微镜下观察细胞移行情况, 随机选取每孔5个低倍视野(100倍)并照相计数越过划线移行的细胞数, 取均值作为移行细胞数。样本量5个, 每一样本重复3次。
取处于对数生长期的人胚眼Tenon’s囊成纤维细胞消化计数后接种于6孔板(5× 106个/孔), 分为对照组(正常培养基)、OPN处理组(0.05、0.5、5 µ mol/L)、OPN和1A12同时处理组(5 µ mol/L OPN+20 µ g/ml 1A12), 铺板24 h后, 换用含1%FBS的DMEM培养基饥饿培养12 h, 处理组按规定的浓度加入OPN和1A12进行刺激, 而对照组加入含1%FBS的高糖培养基, 继续培养1 d后用PBS洗涤1次, 加入1 ml Trizol, 用枪头反复吹打收集于EP管内, 常温静置3~5 min。提取HTFs细胞总RNA, 反转录反应, 采用荧光染料法进行real-time PCR。引物:由上海生工生物工程技术服务有限公司合成。血管内皮生长因子(Vasculer endothelial growth factor, VEGF)上游引物:5′ -CCCTCCGAAACCATGAACTTT-3′ , 下游引物:5′ -AGAGATCTGGTTCCCGAAAC-3′ ; 转化生长因子(Transforming growth factor β , TGF-β )上游引物:5′ -TGCGCTTGCAGAGATTAAAA-3′ , 下游引物:5′ -CGTCAAAAGACAGCCACTCA-3′ 。内参GAPDH上游引物:5′ -ACTCCACTCACGGCAAATTC-3′ , 下游引物:5′ -TCTCCATGGTGGTGAAGACA-3′ 。样本量5个。
取处于对数生长期的人胚眼Tenon’s囊成纤维细胞消化计数后接种于6孔板(5× 106个/孔), 分为对照组(正常培养基组)、OPN处理组(0.05、0.5、5 µ mol/L)、以及OPN和1A12同时处理组(5 µ mol/L OPN+20 µ g/ml 1A12), 铺板24 h后, 换用含1%FBS的DMEM培养基饥饿培养12 h, 处理组按规定的浓度加入OPN和1A12进行刺激, 而对照组加入含1%FBS的高糖培养基, 继续培养1 d后用PBS洗涤1次, 加入300 µ l RIPA裂解液裂解, 用枪头反复吹打收集于EP管内, 然后12β 000 rpm 4 ℃离心20 min后弃沉淀取上清。提取细胞总蛋白后用Bradford法进行蛋白定量, 并测定蛋白浓度。样本量5个。
实验研究。数据采用SPSS 16.0软件进行统计学分析, 计量资料以± s进行描述。对多组数据的比较采用单因素方差分析, 两两组间的多重比较采用LSD-t检验。以P< 0.05为差异具有统计学意义。
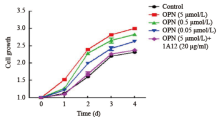
MTT测定法显示, 不同浓度OPN组HTFs细胞增殖差异具有统计学意义(F=174.5, P< 0.01)。随着浓度的增加(0、0.05、0.5、5 µ mol/L), 吸光度值逐渐增加, 各浓度组之间两两比较差异有统计学意义(P< 0.05), HTFs增殖的快慢与OPN的浓度成剂量依赖性。加入OPN单克隆抗体1A12(5 µ mol/L OPN+20 µ g/ml 1A12)后, OPN促进细胞增殖的效应消失, 与对照组相比差异无统计学意义(P> 0.05)。各组分别以0 d的吸光度值作为标化。见图1。
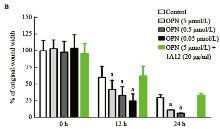
分别于划痕0 h、12 h、24 h时显微镜下观察, OPN可以明显促进HTFs细胞的移行, 随着浓度的增加(0、0.05、0.5、5 µ mol/L), 细胞移行的距离增加, 12 h时各浓度组之间比较差异有统计学意义(F=297.1, P< 0.01)。HTFs细胞移行的距离与OPN的浓度成剂量依赖性。加入1A12(5 µ mol/L OPN+20 µ g/ml 1A12)后, OPN促进细胞移行的效应消失, 与对照组相比差异无统计学意义(P> 0.05)。见图2。
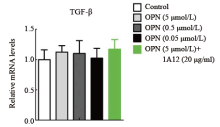
Real-time PCR结果显示应用不同浓度OPN处理48 h后, 对照组、OPN处理组(0.05、0.5、5 µ mol/L)、OPN和1A12同时处理组(5 µ mol/L OPN+20 µ g/ml 1A12)的VEGF和TGF-β mRNA相对表达量差异无统计学意义(P> 0.05), 设定对照组为1.0。见图3-4。
HTFs细胞有少量I型胶原蛋白表达, 随着OPN刺激浓度的增加(0、0.05、0.5、5 µ mol/L), I型胶原蛋白的表达逐渐升高, 不同浓度OPN处理组之间I型胶原蛋白的表达差异具有统计学意义(F=30.2, P< 0.01)。给予OPN抗体1A12后, I型胶原蛋白的表达较OPN处理组(5 µ mol/L)降低, 差异具有统计学意义(P< 0.05)。设定对照组为1。见图5, 红框内表示OPN和1A12同时处理组(5 µ mol/L OPN+20 µ g/ml 1A12)。Tubulin是细胞管蛋白, 是作为内参基因的表达来确定I型胶原蛋白的表达量是否发生改变。
OPN属于细胞外基质蛋白, 首先由Senger于1979年作为一种与恶性转化有关的磷酸化蛋白而提取[1]。它广泛存在于人体各种不同的组织细胞中, 在生理和病理条件下参与细胞粘附、凋亡, 炎症反应, 血管形成, 创面愈合, 骨转换, 肿瘤发生或转移, 免疫应答等过程[2, 3]。OPN分子中有多处高度保守的重要功能区域, 由此OPN与各种不同的细胞表面受体相互作用, 通过信号传导机制引起各种细胞学效应, 从而产生多样化的生理和病理作用[4, 5, 6]。
OPN与多种组织细胞的纤维化密切相关, 发生纤维化的心、肝、肾、肺等器官组织均可检测到OPN的表达明显上调[7, 8, 9, 10]。Wu等[11]研究发现, 在博莱霉素诱导的表皮纤维化小鼠模型中, OPN缺失的小鼠与野生型小鼠相比, 表皮纤维化程度明显较轻, 损伤皮肤区域中的肌纤维母细胞减少; 体外实验也证实OPN缺失的小鼠表皮成纤维细胞的迁移能力下降。体外细胞学研究同样证实了OPN可以调控成纤维细胞的增殖、迁移和重塑过程[12]。尽管之前的研究已经表明OPN在机体的其他部位具有促纤维化的作用, 是调控组织修复和瘢痕形成的重要因子, 但OPN在HTFs中的作用尚不清楚。本研究证实, OPN可以增强HTFs的增殖能力和迁移速度, 并且随浓度升高而增强, 其单克隆抗体1A12则可以抑制这种效应。
HTFs分泌胶原蛋白增加, 是导致青光眼手术后瘢痕形成的重要原因。有研究报道OPN缺陷的小鼠支气管肺泡内的胶原蛋白沉积减少[13]。而过度表达OPN的小鼠肝脏中I型胶原蛋白含量则增加[7]。本研究发现, 随着OPN的浓度升高, HTFs中的I型胶原蛋白的表达也随之上调, 呈浓度依赖性, 而抑制OPN后I型胶原蛋白的表达则下调, 提示OPN可以诱发HTFs中I型胶原蛋白的表达。OPN诱发HTFs中的Ι 型胶原蛋白表达, 这与OPN促进HTFs细胞增殖与移行的表型相符; 而OPN抗体1A12抑制了Ι 型胶原蛋白的表达, 抑制HTFs细胞的增殖与移行。此结果提示可能可以通过调控OPN这个与瘢痕形成相关的重要因子来研发抗青光眼手术中减少瘢痕形成的新药物。
许多学者研究抗青光眼手术局部区域VEGF和TGF-β 的作用, 证实它们参与青光眼滤过手术后瘢痕形成的过程[14, 15]。另有研究报道OPN与VEGF、TGF-β 的表达相关[16, 17]。但在本研究中, 通过Real-time PCR的方法检测了不同浓度的OPN处理后HTFs中的VEGF和TGF-β 的mRNA水平变化, 我们发现给予不同浓度的OPN刺激后, VEGF、TGF-β 的含量均没有明显变化。提示OPN中的不同蛋白序列可能对应激活不同的信号传导通路, OPN在HTFs中发挥其生物学效应过程中并没有激活VEGF、TGF-β 相关的信号传导通路。
综上所述, OPN促进HTFs增殖和移行, 呈浓度依赖性, 该效应可被OPN单克隆抗体1A12抑制。OPN诱导体外培养的HTFs中Ι 型胶原蛋白的表达, 1A12可以抑制这种效应。我们将进一步探索OPN在HTFs中发挥效应的分子生物学机制。
利益冲突申明 本研究无任何利益冲突
作者贡献声明 李维娜:收集数据, 参与选题、设计及资料的分析和解释; 撰写论文; 对编辑部的修改意见进行修改。程金伟:参与选题、设计和修改论文的结果、结论。魏锐利:参与选题、设计、资料的分析和解释, 修改论文中关键性结果、结论, 对编辑部的修改意见进行核修
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|