永存胚胎血管(PFV)是一组与胚胎血管退化失常相关的异常临床表现,如瞳孔残膜、晶状体后纤维血管膜,Mittendorf点、Bergmeister乳头、黄斑发育不全、视神经发育不良、视网膜皱褶等,大部分情况伴有晶状体混浊。由于PFV在临床上比较少见,表现形式又多种多样,是否正确诊断和合理治疗将显著影响患眼的预后。随着二孩政策而来的生育潮,小儿PFV病例可能会有所增加,笔者将从临床表现、诊断、分型、治疗等方面进行阐述,希望能规范该病的诊治并提高疗效。
Persistent fetal vasculature (PFV) is a group of abnormal clinical manifestations associated with the failure of the regression of fetal vasculature. Clinical manifestations can include such conditions as persistent pupillary membranes, persistent posterior fetal fibrovascular sheath of the lens, Mittendorf dot, Bergmeister papilla, macular abnormalities, optic nerve abnormalities, retinal folds and so on, most of which are accompanied by lens opacity. PFV can present in three forms: purely anterior, purely posterior or a combination of both. Due to the scarcity of clinical cases and the heterogeneity of clinical manifestations, an accurate diagnosis and appropriate treatment have a marked effect on a patient's prognosis. With the fertility boom after the second child policy, there may be an increase in the number of children with PFV. The purpose of this review is to discuss the clinical manifestations, diagnosis, types and treatment, to standardize the diagnosis and treatment, and to improve the curative prognosis of PFV.
永存胚胎血管(Persistent fetal vasculature, PFV)是一组与胚胎血管退化失常相关的异常临床表现。在胚胎形成过程中, 玻璃体动脉滋养眼睛的前部, 原始玻璃体动脉的诸多分枝, 分化成虹膜玻璃体血管, 并构建原始玻璃体。通常, 从胚胎第3个月开始, 原始玻璃体动脉及虹膜玻璃体血管开始退化, 胚胎9个月时完全退化。但是在某些病例中, 这些血管系统部分或完全不能退化, 导致晶状体后表面纤维血管膜形成, 表现为后囊膜后出现白色纤维血管化组织, 称为永存原始玻璃体增生症(Persistent hyperplastic primary vitreous, PHPV)[1]。1997年Goldberg[2]提议用更全面的强调病因的名称— — PFV取代 PHPV, 重新定义了这一疾病。PFV较好地描述了与胎儿血管异常有关的一组临床表现, 如瞳孔残膜、晶状体后纤维血管膜、Mittendorf点、Bergmeister乳头、黄斑发育不全、视神经发育不良、视网膜皱褶、视网膜脱离等。文献报道单眼白内障伴PFV的发生率为11%~30%不等[2, 3, 4, 5, 6, 7, 8, 9], 而双眼白内障伴PFV的发生率是2.4%~16.7%[1, 6, 10, 11, 12, 13]。由于PFV属于罕见病, 临床表现形式复杂多样, 正确诊断和合理治疗将显著影响患眼的预后。随着二孩政策而来的生育潮, PFV病例可能会有所增加, PFV导致的原发性和继发性异常多在出生时或出生后数年内出现[14], 故笔者将从临床表现、诊断、分型、治疗等方面进行阐述, 希望能规范该病的诊治并提高疗效。
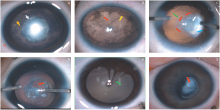
大多数PFV伴有晶状体混浊, 大多表现为晶状体中央区后半部分致密混浊(见图1A), 有时候可以表现为全混浊。因为PFV伴随纤维膜的增殖, 可能突破晶状体后囊膜进入晶状体, 引起晶状体混浊; 也可能由于残留的原始玻璃体动脉牵引, 晶状体后囊膜破裂, 继而导致晶状体混浊。也可能由于纤维血管膜的包绕影响到晶状体的代谢或者其他目前不甚明了的原因, 导致晶状体混浊。
晶状体表面血管表现为晶状体前表面或后表面一条或数条血管, 不伴有纤维膜形成(见图1B)。有时伴有瞳孔残膜。晶状体后纤维血管膜, 可以是一条或多条血管分枝伴有纤维血管膜, 呈现白色或粉红色(见图1C)。异常血管一般来源于睫状体。面积可以小到一个点, 大至覆盖整个晶状体后表面。有时, 由于晶状体后纤维血管膜的增殖和牵引, 可以出现拉长的睫状突。这是典型PFV的表现, 一般是由于晶状体后囊处原始胚胎血管退化失败残留造成的。多数情况下晶状体混浊, 有时也可能是透明的。由于可能影响悬韧带的发育, 有时出现晶状体赤道部切迹而形成脐状凹陷, 甚至晶状体半脱位或全脱位。
指从视神经乳头延伸到晶状体后囊的残余血管, 有时是孤立的一条血管, 有时形成一条索状纤维血管鞘。多数情况伴有晶状体混浊。一般来说, 在妊娠第7个月时, 若玻璃体动脉不能退化, 则会残留成永存玻璃体动脉(见图1D)。
发病机制主要有:①晶状体后纤维血管膜的牵引导致后囊破裂, 房水进入囊袋内引起晶状体膨胀前移, 以致房角关闭; ②另外, 当晶状体后纤维血管膜中心性牵拉睫状突, 造成悬韧带松弛, 导致虹膜隔前移[14], 引起房角变窄; ③虹膜炎症反应和色素脱失播散也可能是继发性青光眼的原因。
瞳孔残膜比较常见, 是指瞳孔区出现类似虹膜样组织残留于瞳孔区, 通常疏松附着于晶状体前表面或跨越过瞳孔缘(见图1E), 有时在瞳孔边缘不影响视力, 有时遮盖大部分瞳孔区而严重影响视觉功能发育。瞳孔区机化膜, 是指瞳孔区出现灰白色伴有或者不伴有血管的纤维血管膜或纤维膜(见图1F), 通常紧密附着于晶状体表面, 部分甚至几乎全部遮盖瞳孔区, 严重影响患儿视功能发育。原因可能是在胚胎发育时未能正常退化的晶状体血管膜的小片残余, 少数情况下, 整个瞳孔会被未退化的中胚层组织遮挡, 这些组织可能显露或不显露其血管性质或起源[2]。董白霞等[15]发现角膜内皮与虹膜色素上皮层在胚胎时期有密切联系, 来自周围的神经嵴细胞沿着视杯前面与角膜内皮之间的间隙进入虹膜基质, 瞳孔残膜或机化膜的形成可能是胚胎血管残余与神经嵴细胞相互诱导所形成。
表现为晶状体后极部一个0.5 mm直径大小的白色的斑点。为原始玻璃体动脉不完全退化所残余, 很少影响视力, 不需要治疗。
Mü llner-Eidenbö ck等[6]提出MFVR是PFV的一种表现形式, 表现为晶状体后极部混浊和后囊膜中央异常, 后囊膜缺损或机化, 这些表现往往是在手术中仔细观察才得以发现, 术前难以经过检测手段了解。如果存在MFVR, 可能对学龄前儿童视功能产生影响。
表现为附在视盘顶端的膜状或短条带状病变。是因为后部玻璃体动脉不完全退化所致。单纯Bergmeister乳头本身不会影响视觉功能, 它对视觉功能的影响主要取决于残留物是否会造成黄斑牵拉。
在某些情况下, PFV还伴有视网膜皱褶, 可能是少量的纤维增生组织沿着Cloquet管附着在视网膜上, 从而导致视网膜褶皱的形成, 在一些严重的病例中, 可能会导致牵拉性视网膜脱离。可发生在任何象限, 发生在黄斑时则影响视力。有时, 残留原始玻璃体动脉的玻璃体附着于视盘上, 增殖牵拉视网膜, 从而导致漏斗状视网膜脱离。PFV可伴随小角膜或小眼球, 与眼球发育受阻有关。
由于PFV临床表现多样, 患儿的综合检查困难, 以及对该病的了解不足, PFV的诊断仍具有挑战性。对于先天性白内障, 术前检查若发现这类胚胎血管, 明确PFV的诊断, 有助于术前手术方案的合理设计。
散瞳后仔细的裂隙灯显微镜检查, 晶状体前面的异常和晶状体后纤维增生成灰白色或粉红色一目了然, 然而连接于视盘和晶状体的原始玻璃体动脉以及眼底病变往往难以查出。这些特征血管的直接可视化是诊断的最佳方法, 国内外大多数报道可使用包括B超、超声多普勒成像、CT、MR成像、和荧光血管造影在内的辅助技术[16, 17, 18]。B超是临床上最常用最快捷的检查, 黄欣等[19]报道其研究中的16眼B超检出率为100%, 然而我们发现, 纤细的血管很难通过B超发现, 多数病例是术中才能明确诊断的。Hu等[18]使用超声多普勒成像胚胎残存血管都显示血液流动。
所以, 对于先天性白内障患者术前, 必须先进行散瞳裂隙灯显微镜检查。有条件的医院建议使用超声多普勒检查。
Pollard[20]率先提出:根据所涉及的位置, PFV可为3种类型:前部型、后部型、混合型。前部型PFV, 占所有病例的25%左右; 主要表现为白内障和晶状体后纤维血管膜性混浊, 有些也存在浅前房、晶状体悬韧带松弛, 睫状突拉长; 少数病例可能发生继发性闭角型青光眼。后部型PFV, 主要涉及玻璃体和视网膜, 约占12%; 主要表现为永存玻璃体动脉、视网膜皱褶以及视网膜脱离等。混合型PFV在临床中最常见, 约占所有病例的60%, 临床表现涵盖前后段。
这一分型涵盖了大部分PFV的表现形式, 被大家广为接受, 很长一段时间内指导了临床诊断和治疗。2016年, Hu等[18]通过Retcam、B超、多普勒成像检查, 将混合型PFV根据形态进行分型, 分成I型、Y型、倒Y型、X型, 以此四分型指导手术治疗。I型和Y型主要累及前段, 后两型前后段均受累。根据这一分型, I型和Y型, 可以通过眼前节手术治疗, 而对于倒Y型、X型, 要充分评估解剖恢复的可能性以及视功能恢复的可能性, 谨慎选择治疗方案。
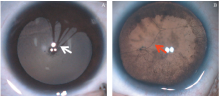
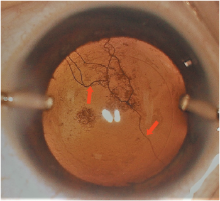
我们根据PFV病变和晶状体的相对位置以及血管残留伴随纤维血管膜的情况, 排除眼底严重合并症如合并视网膜皱襞以及视网膜脱离等之后, 将主要累及眼前段的PFV分为3级, 这个分级有利于指导眼前段手术时机和治疗方案的决策。1级:瞳孔残膜, 瞳孔区机化膜, 或者晶状体前表面存在不伴有纤维膜的血管, 三者之一或合并存在(见图2); 2级:晶状体后囊膜后存在不伴有纤维膜的血管(睫状体来源的血管或血管网, 视盘来源的血管, 两者之一或合并存在) (见图3); 3级:晶状体后伴有纤维血管膜, 可同时合并有1级或2级的临床表现(见图1C)。
PFV目前主要的治疗方法为手术治疗, 多数学者提倡早期行晶状体后纤维增殖膜切除与玻璃体切割[21, 22, 23], 有效的手术治疗联合弱视治疗可使患儿获得尽可能多的有用视力, 并能避免严重并发症的发生。
婴幼儿先天性白内障合并PFV行手术治疗的目的是重建视觉通道, 植入人工晶状体, 减少PFV引起的后续并发症。随着微创玻璃体技术的发展, 可以采用玻璃体切割头(23G、25G等)行晶状体切除联合前段玻璃体切割术, 术中进行前囊环形切除, 皮质吸除, 后囊环形切除, 纤维血管膜切除, 前段玻璃体切割, 如果一期手术时年龄合适, 联合人工晶状体囊袋内植入。
手术过程中, 前囊切除和皮质吸除同常规晶状体切除术。后囊膜有时是和晶状体后纤维血管膜连成一体的, 有时还伴随后囊膜前方的盘状机化膜, 可以用玻璃体切割头切除机化增殖膜和纤维血管膜, 遇到特别坚韧增厚的纤维膜且范围特别大时, 可以用锋利的刀头或针头斜面先切破纤维膜, 然后再使用玻璃体切割头切除纤维膜和前段玻璃体, 切除后囊膜形成3 mm直径中央孔。以便同期或二期将人工晶状体植入囊袋内, 以保持长期的位置稳定性。笔者发现, 存在广泛晶状体后纤维增生的患儿, 往往是来自睫状体的血管伴纤维膜增生, 中央切除之后, 血管膜和睫状体之间的牵拉解除, 周边残留的纤维血管膜具有逐渐向周边收缩的趋势, 中央切除区会逐渐扩大。所以, 在这些病例, 我们认为做成3 mm直径的中央孔比较合适, 尤其是一期不植入人工晶状体的患者, 保留好周边囊袋以备将来二期人工晶状体囊袋内植入。
前部PFV中, 晶状体后纤维血管膜, 常常有许多血管分枝甚至纠缠成团。后部PFV中, 连接视盘和晶状体后囊的血管通常只有一条或者发出数条分枝连成纤维血管鞘。一些学者介绍了他们的处理方式, 切除晶状体和前段玻璃体, 保留血管蒂偏向一侧的部分囊膜和悬韧带, 使血管蒂进一步偏向该侧以暴露视轴中心区[16, 17, 18]。这些血管, 正如文献证实如果有血液流通的, 在被切断后可能会出血。可以在准备切断血管前, 提高灌注压, 大部分情况下可以做到不出血或者少量出血后自动止血, 如果还是有出血, 可以采用水下电凝的方法止血。那么通向视盘的这条血管或者血管鞘, 需要切到什么位置才合适呢?实际上, 我们在做前段玻璃体切割时, 显微镜所能聚焦清晰的范围是在前段玻璃体, 本着最小损伤的原则, 我们只要在显微镜显示清晰的前段玻璃体范围内切断血管就可以了, 血管残端会自动退缩回后段玻璃体内, 不会造成任何并发症。
对于PFV -1级的患者, 如果不合并先天性白内障, 要根据残膜或机化膜或血管和视轴区的相对位置来确定手术时机。①如果瞳孔残膜疏松附着于晶状体表面, 除非非常严重致密, 一般不会严重影响透光度, 不会造成严重弱视, 可以随访观察, 待患儿长大些再酌情处理。②如果是机化膜则可能会紧密附着于晶状体表面而且伴随有瞳孔不规则后粘连, 范围小不影响视轴区时可以随访观察, 而很多时候范围很大且严重遮挡视轴区, 需要尽早手术切除, 这种情况一般不伴有白内障, 术中要注意保护好透明晶状体。③晶状体前表面的血管若单独发生, 一般不影响视力, 可不处理。
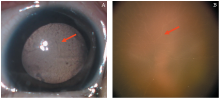
对于PFV-2级的患者, 临床上见到的患者常常伴有严重白内障, 在手术清除混浊皮质后才显示出异常血管, 这种情况术中可以切除中央区后囊膜形成一个约3 mm的孔, 周边的血管残端可以置之不理。偶尔, 也有一些患儿表现为晶状体完全透明, 晶状体后存在血管网却不伴纤维增生膜(见图4), 这种情况宜随访。Goldberg[2]观察到几例未手术患者的晶状体后血管数年后血流终止, 出现白线化。
对于PFV-3级的患者, 大多数情况伴有晶状体混浊, 严重影响视功能发育, 需要尽早手术。有时候, 即使晶状体透明, 广泛的晶状体后纤维血管膜有如白内障一样严重影响视功能发育, 也需要尽早手术。偶尔, 晶状体后纤维膜存在但是远离视轴区, 晶状体透明, 这种情况可以随访观察。
瞳孔残膜或机化膜严重时需要手术切除。很多时候不合并先天性白内障, 仅需分离粘连, 剪除残膜或机化膜, 尽可能恢复瞳孔视轴区透光即可。若机化膜严重且伴瞳孔后粘连, 为了防止全周后粘连出现瞳孔阻滞性青光眼的可能, 在做机化膜切除手术时有必要做一个虹膜周边切除。
对于合并视网膜病变的PFV, 则需要全面的功能和解剖学的评估, 方能决定治疗方案。
手术只是建立视觉通道的必要措施, 术后的视觉康复训练非常重要。尤其是, 合并PFV的白内障大部分都是单眼发病, 这给弱视训练带来了很大的挑战。需要医师、患者家属、患者三方联动, 加强健眼的遮盖, 患眼的屈光矫正和训练, 持之以恒, 方能获得理想的视功能康复。很多文献都表示PFV患者预后不良, 视力恢复非常有限, 这和患者接受治疗的年龄偏大, 弱视严重有关, 也和PFV后续继发表现加重, 如继发性青光眼、牵拉性视网膜脱离等有关[19, 20, 21, 22, 23]。笔者曾经报道23岁的成人混合型PFV合并白内障, 不伴视网膜病变, 手术后获得右眼0.2左眼0.5的视力[24]。提示我们应该仔细评估, 积极治疗, 不能因年龄过了发育敏感期就放弃。
PFV是一组与胚胎血管退化失常相关的异常临床表现, 大部分合并先天性白内障, 表现形式多种多样, 有些时候隐匿难发现, 故先天性白内障术前散瞳检查和影像学检查是必要的。PFV传统上分为3种类型:前部型、后部型、混合型。2016年有作者提出对于后部或混合型PFV细分为四型:I型、Y型、倒Y型和X型。我们将主要累及眼前段的PFV分为3级:1级:瞳孔残膜或机化膜, 晶状体前表面不伴有纤维膜的血管, 三者之一或并存; 2级:晶状体后囊膜后存在不伴有纤维膜的血管(睫状体来源的血管或血管网, 视盘来源的血管, 两者之一或合并存在); 3级:晶状体后伴有纤维血管膜, 可同时合并有1级或2级PFV。这些分型分级综合思考, 有助于我们在临床上进行手术时机、手术方式甚至手术与否的决策。微创白内障手术和玻璃体切割术的进展, 为早期婴幼儿手术提供了更安全的保障, 而PFV术后弱视训练的正规管理对视觉康复极为重要。
利益冲突申明 本研究无任何利益冲突
作者贡献声明 赵云娥:参与选题、设计和修改论文, 根据编辑部的修改意见进行核修。胡曼:收集数据, 剪辑图片, 参与文献资料的收集及分析
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|