增殖性糖尿病视网膜病变(Proliferative diabetic retinopathy, PDR)是引起糖尿病患者视力下降和盲的重要原因[1]。在欧美发达国家因糖尿病防控体系完备, PDR比例日益降低(2.1%~2.5%)[2]。然而, 在我国特别是欠发达地区PDR屡见不鲜, 全国平均水平为3.3%~7.4%[3, 4], 在西部地区最高可达20%[5]。
在临床实践中很多PDR患者经历了玻璃体切除手术以及全视网膜光凝(Panretinal photocoagu-lation, PRP)治疗, 视力和视觉功能仍然很差, 处于法定盲的边缘。这类患者虽然已经控制住了视网膜增殖病变的发展, 但常常合并明显的糖尿病黄斑水肿(Diabetic macular edema, DME), 临床治疗效果较差。笔者回顾文献尚未发现这类患者视力影响因素的报道。因此, 通过回顾性研究, 对这些问题做一探讨。
激光治疗后DME为增殖性糖尿病视网膜病变经3~5次视网膜激光热凝治疗后, 经光学相干断层扫描(OCT)/眼底荧光素血管造影(FFA)检查仍有明显的黄斑水肿者。
纳入标准:符合以上定义, 且随访资料完备, 可供分析的病例, 均纳入本次研究; 患者年龄在18岁以上, 无性别限制, 无糖尿病类型(1型或2型)限制, 无病程限制。排除标准:①PDR经视网膜光凝治疗后不合并DME者; ②虽符合上述定义但无完整的随访资料者; ③患眼因屈光介质不清, 提供的眼底图像资料模糊不能辨认者; ④患眼合并新生血管青光眼、视网膜脱离未复位等可能严重干扰本次结果分析者; ⑤其他疾病导致的黄斑水肿如视网膜中央/分支静脉阻塞等。
收集2015年1月至2016年12月在绵阳万江眼科医院门诊治疗符合纳入标准者共30例(43眼)。其中男18例, 女12例, 平均年龄(63.7 ± 5.6)岁, 单眼17例, 双眼13例。合并高血压21例, 高血脂17例, 肾功能不全3例, 尿毒症透析者1例。43眼中有玻璃体割手术史29眼, 玻璃体割手术前主要合并症为:玻璃体积血13眼, 纤维血管膜形成12眼, 牵拉性视网膜脱离4眼。
采用国家标准对数视力表测量所有患者的最佳矫正视力(BCVA)[6]。
眼底照相及荧光素血管造影为同一台设备。从储存影像资料的磁盘数据库中提取纳入病例的图像, 由2名研究者独立进行读片, 分析眼底彩照、自发荧光及荧光造影图像, 主要对黄斑水肿程度定性判断, 观察有无渗漏和周边视网膜有无残余无灌注区, 有无合并黄斑缺血及糖尿病视神经病变。如读片结果不一致则由2位读片者商讨后再下结论。
分析每例患者的OCT(OCT-2000, 日本拓普康公司)图像。测量指标判定标准如下[7]:
①黄斑中心厚度(Central macular thickness, CMT):使用计算机内置软件测量黄斑中心区域(直径1 mm)从玻璃体视网膜界面到视网膜色素上皮(RPE)层外边界的平均值。
②黄斑水肿囊腔大小测定及分级方法:采用计算机内置软件的卡尺手动测量囊腔各个径线上的直径, 选择最大直径作为判断标准。参照黄斑裂孔大小的分级方法, 以囊腔各径线最大直径≥ 350 μ m为大囊腔, 小于< 350 μ m为小囊腔。
③黄斑水肿的位置分为:中心凹内水肿和旁中心水肿(中心凹500 μ m外)。
④微小浆液性视网膜脱离定义为:神经上皮抬高, 神经上皮和RPE之间出现光学可见间隙或空间。
回顾性系列病例研究。采用SPSS 20.0统计学软件进行数据分析。年龄、BCVA、CMT等计量资料用$\bar{x}^{..}\pm^{..}s$表示。根据DME的每个影像学特征分亚组。两组比较采用独立样本t检验, 多组比较用单因素方差分析, 样本率和构成比的比较常用R× C表资料的卡方检验。以P < 0.05为差异有统计学意义。
30例(43眼)DME患者平均BCVA为3.98 ± 0.58。其中对数视力表4.5以下的低视力眼有31眼(72.1%, 31/43), 法定盲有9眼(20.9%, 9/43)。4.5以上相对好的视力12眼仅占27.9%(12/43)。
30例(43眼)DME患者治疗前平均CMT值为(391 ± 130)μ m, 其中200~300 μ m 11例, 400~500 μ m 24例, 500~700 μ m 6例, > 700 μ m 2例。
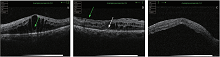
OCT下可见高度的水肿形成大小不等的囊腔, 形态各异。43眼黄斑水肿中囊腔直径大于350 μ m的大囊腔有22眼, 占51%; IS/OS层(椭圆体带)破坏比例极高, 为81%; 囊腔或水肿位置为旁中心的占37%; 合并黄斑前膜占21%, 7眼合并中心凹下微小浆液性视网膜脱离, 1眼因近期补充视网膜光凝后出现明显的渗出性视网膜脱离。见图1。
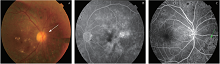
眼底照相可见周边视网膜的激光斑(已色素化), 黄斑水肿明显, 可伴有明显的出血斑和渗出, 渗出呈环形、花瓣型或仅在黄斑某一侧。合并糖尿病视神经病变者眼底表现为视盘蜡黄色, 部分患者有视神经凹陷加深甚至杯盘比(C/D)扩大, 本研究中合并糖尿病视神经病变6眼, 占13.9%(6/43)。见图2。
FFA下可见黄斑区微动脉瘤、黄斑区囊样的荧光渗漏或着染, 少数可合并黄斑的缺血、毛细血管拱环扩大, 周边视网膜陈旧性激光瘢痕导致的遮蔽荧光。部分患者残留周边视网膜少许无灌注区未封闭。43眼中有4眼合并周边视网膜无灌注区, 需补充激光, 占9.3%(4/43)。见图2。
参照全球糖尿病视网膜病变项目小组简化了的DME分级标准[8]。43眼中轻度黄斑水肿13眼, 占30%; 中度黄斑水肿19眼, 占44%; 重度黄斑水肿11眼, 占26%。
DME的临床特征中椭圆体带是否破坏、黄斑水肿是否位于黄斑中心、黄斑水肿囊腔的大小、水肿的程度以及是否合并糖尿病视神经病变5种临床特征各自亚组间BCVA比较差异有统计学意义(P < 0.05), 表明这些因素可能对DME的视力有较大影响。而是否合并黄斑前膜、是否合并微小视网膜脱离(Retinal detachment, RD)以及是否合并周边视网膜无灌注区3个临床特征各自亚组间BCVA比较无统计学差异(P > 0.05), 表明这些因素可能对DME的视力影响相对较小。见表1。
| 表1 糖尿病性黄斑水肿临床特征与BCVA关系分析 Table 1 Relations between clinical features in BCVA of DME |
DME可以发生在糖尿病视网膜病变的任何阶段, 既可以发生在非增殖期也可以发生在增殖期[9]。进入增殖期以后, 治疗的重点在于及时有效的PRP治疗以控制增殖的发展。激光治疗后黄斑水肿是普遍存在的, 现有的文献对于这一时期的DME并无系统研究。
DME的实质是黄斑区血浆物质渗漏或脂质沉着导致的视网膜变厚, 当增厚的部位发生在黄斑中心或临近中心的位置, 患者就会发生视物变形或视力下降[10]。
回顾DME形成的机理, 总体与高血糖有重要关系。高血糖诱导的糖尿病视网膜病变的发病机制与4个主要的生化途径有关:多元醇代谢通路、晚期糖基化终末产物通路、蛋白激酶C通路、氨基己糖通路[11]。所有这些通路都导致氧化应激增加、炎症反应和血管功能紊乱。氧化应激和炎症反应又导致生长因子和细胞因子, 从而打破血视网膜屏障(Blood-retinal barrier, BRB)导致DME的发展[12]。除此以外, 近年的研究发现糖尿病视网膜上神经血管单元也发生了代谢和退行性改变[13]。很多学者认为BRB破坏形成水肿会导致血管神经单元的外环境破坏造成细胞凋亡、神经细胞丢失, 而细胞凋亡又会加重BRB的破坏, 形成恶性循环。
激光治疗后DME的病理机制在以上阐述的范围以内又有新的特点。因为视网膜光凝治疗后可以增加视网膜内含氧量; 减少血管活性因子和初始的血管内皮细胞生长因子; 并且可以加强RPE细胞和胶质细胞的吞噬作用。最近的一份研究表明RPE细胞在激光灼烧的边缘通过光感受器调节各种细胞因子。但这类DME的病程大多很长, 视网膜内部结构破坏严重, 视网膜光感受器、椭圆体带以及视网膜血管神经单元都有不同程度的破坏, 视网膜及其血管神经单元中细胞丢失更多, 残存功能差。视网膜处于长期的炎症状态甚至激发了机体的免疫系统应答机制参与其中[14], 使病程迁延不愈, 病理机制更加复杂, 导致DME长期存在。
本研究为回顾性临床试验, 对其病理机制没有更多深入的研究。研究中主要借助了OCT和FFA来帮助观察和评判DME的程度和细微结构[15]。通过OCT自带计算机软件直接测量CMT和黄斑囊样水肿囊腔的大小, 利用OCT的高分辨率可以清楚分析视网膜各层次的损害。因椭圆体带和视网膜光感受器直接相关, 其破坏后对视力影响较大[16]。故本研究重点观察了患眼椭圆体带破坏的情况, 同时观察和分析了黄斑下微小视网膜脱离、黄斑水肿的位置等指标, 为归纳出这类DME的临床特征规律提供了依据。
研究中使用的另外一个重要工具是FFA, 它的优点在于能了解病灶渗漏的情况, 使治疗时靶点更准确, 并能发现遗漏的无灌注区和周边的异常血管[17], 使治疗变得及时和有针对性, 并能鉴别是否合并糖尿病视神经病变和黄斑缺血, 可以弥补眼底检查和OCT的不足。
根据OCT和FFA影像学研究发现, 总结激光治疗后DME影像学特征为:中、重度黄斑水肿比例大(70%), 水肿或囊腔位于中心凹比例大, 对视网膜外层结构(椭圆体带及外界膜)破坏严重, 部分患者可合并黄斑下微小浆液性视网膜脱离、黄斑前膜和缺血性视神经病变。在这些特征中以椭圆体带破坏, 黄斑水肿位于黄斑中心、黄斑水肿囊腔的大小、水肿的程度以及合并糖尿病视神经病变5个因素对患者的视力有较大影响, 而合并前膜、合并微小RD以及合并周边视网膜无灌注区3个因素对患者视力影响相对较小。
以上结论来自于回顾性临床资料, 只对该问题的深入研究提供了一种思路, 尚需更多大数据资料和随机对照试验研究加以验证。
利益冲突申明 本研究无任何利益冲突
作者贡献声明 乔岗、曹奎:收集数据, 参与选题、设计及资料的分析和解释; 撰写论文; 根据编辑部的修改意见进行修改。董万江:参与选题、设计和修改论文的结果、结论。邹强性、何春梅:参与选题、设计、资料的分析和解释; 修改论文中关键性结果、结论; 根据编辑部的修改意见进行核修
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|