第一作者:向圣锦(ORCID:0000-0001-5879-0381),xsj4228@163.com
目的 探讨红景天苷(Sal)对视网膜神经节细胞(RGCs)凋亡的抑制作用。方法 实验研究。36只C57BL6J小鼠随机分为空白组、模型对照组、不同浓度Sal实验组,每组6只,均以右眼为实验眼。空白组仅注射0.9%PBS溶液,模型对照组和实验组玻璃体腔注射N-甲基-D-天(门)冬氨酸(NMDA) 1.5 μl建立RGCs损伤模型;建模前48 h,模型对照组注射1.5 μl 0.9% PBS溶液,实验组玻璃体腔注射不同浓度Sal(0.1、0.4、2、8 mmol/L,1.5 μl)。建模5 d后制备视网膜标本,观察视网膜RGCs存活及凋亡情况,Western Blot法检测视网膜中Caspase-3、Caspase-8蛋白的表达。数据采用单因素方差分析。结果 HE染色显示空白组视网膜RGCs无变化,模型对照组RGCs显著减少,不同浓度Sal实验组RGCs细胞核染色数目较模型对照组逐渐增加,并呈浓度依赖性;经视网膜平铺片测定RGCs存活情况,发现空白组RGCs正常存活,模型对照组仅少量RGCs存活,不同浓度Sal组RGCs存活率较模型对照组提高,各组小鼠RGCs阳性细胞数比较差异有统计学意义( F=212.0, P < 0.001)。同时,8 mmol/L浓度的Sal实验组Caspase-3、Caspase-8蛋白表达明显低于模型对照组,差异有统计学意义( F=168.3, P < 0.001)。结论 Sal可以抑制NMDA介导的RGCs凋亡,对RGCs损伤有保护作用。
Objective: To determine the neuroprotective effects of salidroside (Sal) on murine retinal ganglion cell (RGC) apoptosisinduced by N-methyl-D-aspartate (NMDA).Methods: Thirty-six C57BL6J mice were randomized into a blank normal control group, a model control group, and four experimental group ( n=6 each). The right eyes of the experimental groups received a 1.5 µl intravitreal injection 0.1, 0.4, 2, or 8 mmol/L Sal ( n=6 mice for each dose) 48 hours before NMDA was injected, and phosphate-buffered saline (PBS, 1.5 µl) were injected intravitreally in the model control group 48 hours before NMDA was injected. Intravitreal NMDA injections (1.5 µl at 0.1 mmol/L), were then performed in the model control group and in the experimental groups. PBS (1.5 µl) was injected intravitreally in the blank control group. Retinas derived from the mice were flatmounted and stained with hematoxylin and eosin to identify the RGCs. The number of RGCs was compared between NMDA and PBS-injected eyes for all groups. The levels of caspase-3 and caspase-8 were analyzed by Western Blot. Data were analyzed using ANOVA.Results: Compared with the blank model group, NMDA induced a significant increase of RGC apoptosis in the model control group and in the experimental groups. Compared with the model control group, Sal significantly inhibited RGC apoptosis in a dose-dependent manner ( F=212.0, P<0.001), and the protein expression of caspase-3 and caspase-8 was significantly down regulated ( F=168.3, P<0.001).Conclusions: Sal inhibited NMDA-induced RGC apoptosis and provided some neuroprotective effect for glutamate-mediated RGC excitotoxicity.
青光眼是一组由病理性眼内压升高或者视神经血流灌注压降低等多种因素引起的视神经退行性疾病, 它是导致不可逆性致盲性眼病的第二大病因[1]。近年来的一系列临床研究, 如“ 进展期青光眼干预研究” (Advanced glaucoma intervention study, AGIS)[2]、“ 早期青光眼协作治疗研究” (Collaborative initial glaucoma treament study, CIGTS)[3]、“ 早期青光眼治疗研究” (Early manifest glaucoma trial, EMGT)[4]及“ 低眼压性青光眼治疗研究” (Low pressure glaucoma treatment study, LoGTS)[5]的临床数据表明, 降低眼压并不能阻止所有青光眼(尤其是正常眼压性青光眼)的病程进展, 如AGIS研究结果显示, 在已经达到“ 靶眼压” 水平的患者中, 仍有部分患者的视野继续丢失, 充分说明青光眼视神经保护治疗的必要性, 这为青光眼的“ 视神经保护” 治疗提供了确凿有力的证据, 并成为研究热点。
由于青光眼视神经损伤发生机理的复杂性, 多靶点药物对于青光眼视神经损伤具有很好的应用价值[6]。中药化学成分复杂多样, 能同时从多层次、多靶点、多机制对抗青光眼的视神经损伤, 显示出中医药在青光眼视神经保护方面的优越性。大量的研究证实, 中药通过抑制自由基产生, 提高抗氧化应激损伤能力; 降低谷氨酸浓度; 改善视神经轴浆运输; 改善视盘和视网膜血液循环; 抑制神经细胞凋亡; 促进视网膜神经节细胞(Retinal ginglion cells, RGCs)轴突再生等多个环节起到视神经保护作用[7]。我们也在试验中发现, 中药红景天的主要有效成分红景天苷(Salidroside, Sal)对谷氨酸兴奋性毒性导致的RGCs凋亡具有较好的的保护作用, 现报告如下。
1.1.1 实验动物 36只8周龄健康雌性C57BL6J小鼠, 体质量20~30 g, 由北京维通利华实验动物技术有限公司提供[批号:SCXK(苏):2016-0003], 经温州医科大学动物伦理委员会批准(伦理批号:wydw2017-0513)。所有小鼠经眼科常规检查排除眼部疾病, 饲养于实验动物中心, 保持室温25 ℃, 予以12 h/12 h的昼夜节律, 光照强度为500 lx, 给予充足的食物和水分。
1.1.2 主要试剂及仪器 Sal(中国食品药品检定研究院, 纯度≥ 98%); N-甲基-D-天(门)冬氨酸(N-methyl-D-aspartate, NMDA) (Selleck, S7072); Tunel凋亡荧光染色试剂盒, 普洛麦格(北京)生物技术有限公司; 转录因子Brn3-b微管蛋白β -Ⅲ -tubulin抗体(艾博抗上海贸易有限公司, ab78078, 小鼠单抗, 1∶ 1 000); Cleaved Caspase-3抗体(美国SCT公司, 9664 s, 1∶ 500); Cleaved Caspase-8抗体(美国Life technologies公司, 710535, 1∶ 1 000); 荧光488山羊抗兔二抗(美国Life technologies公司, A11001, 1∶ 1 000); HRP标记山羊抗兔二抗IgG(美国SANTA Cruz公司, sc-2004, l∶ 1 000); HRP标记山羊抗小鼠二抗IgG(美国SANTA Cruz公司, sc-2005, l∶ 1 000); 质量分数0.5%盐酸丙美卡因滴眼液(美国爱尔康公司); 妥布霉素地塞米松滴眼液(美国爱尔康公司); Hamilton显微注射针带33 g针头(瑞士Hamilton公司); 体视显微镜和荧光显微镜(德国莱卡公司); 电泳仪与成像系统[伯乐生命医学产品(上海)有限公司]。
1.2.1 实验动物的分组 将36只实验小鼠按照随机数字表法分为空白组、模型对照组和4个不同浓度Sal实验组, 共6组, 每组6只。实验前正常条件饲养、观察1周。
1.2.2 谷氨酸兴奋性毒性模型建立以及药物干预 通过玻璃体腔注射法建立小鼠谷氨酸兴奋性毒性模型。所有小鼠造模前用复方托品酰胺滴眼液充分散瞳, 10%磺胺醋酰钠滴眼液冲洗结膜囊, 用质量分数4%水合氯醛腹腔内注射麻醉, 剂量为10 m1/kg, 选取右眼用0.5%盐酸丙美卡因滴眼液点眼行表面麻醉, 用Hamilton 33G注射针头于颞侧角膜缘后2 mm处向玻璃体中央刺入, 在直视下模型对照组和实验组注入浓度为100 μ mol/L的NMDA 1.5 μ l, 空白组注入PBS 1.5 μ l术后妥布霉素地塞米松滴眼液点眼。
药物干预:在造模前48 h, 实验组玻璃体腔注射质量浓度分别为0.1、0.4、2、8 mmol/L的Sal各1.5 μ l预处理, 模型对照组玻璃体腔注射PBS 1.5 μ l预处理, 空白组不处理。玻璃体腔注射方法同前述造模方法在同一眼颞侧角膜缘后2 mm处相同位置注入。期间去除术后白内障等并发症小鼠, 每组实验动物若有死亡则及时补充。
1.2.3 组织病理学检查 造模5 d后小鼠过量麻醉致死, 迅速取出各组小鼠右眼眼球, 4%多聚甲醛溶液浸泡固定24 h, 然后组织脱水、石蜡包埋, 每组随机选择3只眼球沿冠状面行4 μ m连续切片, 苏木精— — 伊红染色(HE染色)后于200倍光学显微镜下观察并拍照, 观察RGCs死亡及存活情况。另外3只眼球视网膜β -Ⅲ -tubulin免疫荧光染色后, 平铺片检测RGCs存活情况。
1.2.4 Western Blot法检测视网膜中Caspase家族蛋白的表达 取视网膜标本后加入RIPA裂解液, 匀浆器充分匀浆, 冰上裂解15 min。4 ℃下17 850 r/min
离心10 min, 收集上清并测定蛋白质浓度。每孔取50 μ g蛋白行SDS-PAGE电泳, 并将蛋白转印到PVDF膜上, 5%脱脂奶粉封闭后加入一抗, 4 ℃孵育过夜, TBST洗膜3次, 加入二抗, 室温孵育l h, TBST洗膜3次, ECL显色, 拍照。对图像进行灰度值分析, 以β -actin为内参, 计算目的蛋白灰度值。
实验研究。采用SPSS 22.0统计学软件进行数据分析。所有结果用 ± s来表示。各组间比较采用单因素方差分析。所有统计检验均采用双侧检验。以P < 0.05为差异有统计学意义。
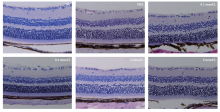
各组经HE染色, 空白组小鼠视网膜RGCs细胞数量和形态正常; 模型对照组GCL层细胞数明显减少, 视网膜厚度变薄; 不同浓度Sal预处理组则随着浓度增加, RGCs细胞核染色数目较模型对照组逐渐增加(见图l)。
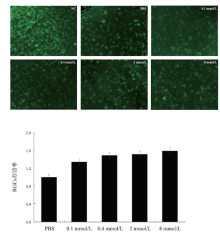
各组经视网膜β -Ⅲ -tubulin免疫荧光染色后平铺片, 检测RGCs整体存活情况, 发现空白对照组小鼠视网膜RGCs大量存活, 模型对照组仅少量RGCs存活, 不同浓度Sal组RGCs存活率较模型对照组提高, 并呈一定的浓度依赖性, 即浓度越高, 存活率越高(见图2)。各组小鼠RGCs阳性细胞数明显不同, 差异有统计学意义(F=212.0, P< 0.001); 与模型对照组相比, 不同浓度实验组小鼠RGCs阳性细胞数逐渐增多, 并呈一定的浓度依赖性, 0.1、0.4、2、8 mmol/L浓度实验组较模型对照组RGCs存活率分别提高34%、48%、51%、59%, 差异均有统计学意义(P< 0.05) (见图2)。
空白对照组Caspase-3、Caspase-8不表达, 模型对照组小鼠视网膜中Caspase-3、Caspase-8蛋白表达较强, 实验组小鼠视网膜凋亡蛋白Caspase-3、Caspase-8表达显著下调。模型对照组与8 mmol/L Sal预处理组视网膜中Caspase-3、Caspase-8蛋白表达差异有统计学意义(F=168.3, P < 0.001), 见图3。
青光眼发病机理复杂, 导致青光眼性视神经病变的主要病理机制是RGCs凋亡, 目前的研究表明, 无论是细胞凋亡的外源性通路、还是内源性通路均参与了青光眼RGCs凋亡的全过程, 且相互作用, 加速细胞的凋亡活动[8]。而诱发青光眼神经节细胞凋亡的主要因素包括神经营养因子的剥夺、谷氨酸兴奋性毒性作用、线粒体功能失调、氧化应激、神经胶质细胞活化以及炎症反应等[9, 10]。其中, 谷氨酸兴奋性毒性被认为是神经损伤的最终途径, 与青光眼的RGCs损伤密切相关[11, 12]。在高眼压等病理状态下视网膜谷氨酸局部浓度显著增高, 成为兴奋性毒素, 激活了RGCs上的兴奋性氨基酸受体(在哺乳动物, 主要是NMDA受体, 是介导神经毒性损伤最主要的受体), 引发大量的Ca2+内流, 导致细胞内Ca2+超载, 通过一系列胞内级联反应, 最终导致RGCs凋亡或死亡[12]。
正是因为谷氨酸兴奋性毒性在青光眼RGCs凋亡中的重要作用, 许多青光眼视神经保护研究均选择应用NMDA介导RGCs损伤来建立细胞或动物模型来研究药物疗效以及发病机理[13, 14, 15]。因此, 我们应用NMDA玻璃体腔注射建立青光眼RGCs损伤模型, 可以既经济又便捷的构建RGCs损伤模型。该模型可以用于青光眼特别是正常眼压性青光眼的视神经保护研究[16]。在既往的试验中, 我们发现, 8周龄C57BL6J小鼠玻璃体腔注射0.1 μ mol/0.15 μ L的NMDA即可在注射后5 d出现大量的RGCs死亡, 因此, 本实验选择此浓度和剂量研究Sal对青光眼RGCs凋亡的抑制作用。
Sal是从红景天属植物中分离得到的糖氧苷类化合物, 广泛存在于红景天属植物中, 具有益气活血, 润肺补肾等功效。现代药理学研究表明, Sal具有广泛的药理活性, 可以发挥抗衰老、耐缺氧、抗疲劳、抗辐射、增强免疫力、抗肿瘤、防治心血管系统疾病等多种药理作用[17]。近年来研究发现, 在体外培养的多种神经细胞, Sal能以剂量依赖性方式显著抑制由氯化钾和谷氨酸诱导的Ca2+内流的过度增加, 并抑制Ca2+的释放, 产生抗谷氨酸兴奋性毒性从而发挥神经保护作用[18, 19], 而谷氨酸兴奋性毒性损伤在参与神经退行性疾病神经细胞死亡中起着关键作用[20]。除了降低谷氨酸兴奋性毒性以外, Sal还具有强大的抗氧化损伤能力, 还可以通过多种途径抑制氧化应激所致的多种神经细胞凋亡, 在神经退行性疾病中, 可以起到较好的保护神经元作用[21, 22, 23]。
同老年性痴呆、帕金森病一样, 青光眼亦属于神经退行性疾病, 以神经元轴突损伤为主要病例特征。而且视网膜为脑组织延伸, RGCs为其重要神经元, 理论上Sal对其也有较好的保护作用。我们选择NMDA介导的RGCs损伤模型实验也进一步证实了Sal可以起到较好的保护RGCs作用, 并呈一定的剂量依赖性。Sal主要通过抑制RGCs的凋亡来保护RGCs损伤, 但Sal是通过何种机制抑制RGCs的凋亡从而起到神经保护作用, 仍然需要进一步的研究证实。
另外, 需要指出的是, 以往的大多数药物抑制RGCs凋亡的实验研究均采用离体培养原代细胞的方式在体外进行, 筛选出的有效药物再以口服方式在模型动物体内进一步证实其效果和机理研究。但由于体内环境的是一个复杂的多因素系统以及血-眼屏障的存在, 致使部分在体外细胞实验中有效的药物, 在体内动物实验中并不能获得预期结果, 或全身大量用药而导致其他不良反应。而玻璃体腔注药可以使药物直接作用于病变部位, 即使微量也可产生高效; 而且玻璃体内无血管, 需依靠房水循环来完成物质代谢, 可以较长时间维持有效的治疗质量浓度; 同时, 玻璃体腔内注药不需要经过全身代谢, 可以避免全身用药的不良反应; 另外, 由于眼内复杂代谢条件下的研究结果较体外细胞实验结果更可靠, 因此玻璃体腔注射是一种比较理想的给药方式。Burugula等[24]在研究姜黄素对RGCs凋亡的抑制作用时即采用了玻璃体腔注射的方法, 获得了理想的研究结果, 这充分说明这种方法的可靠性和可行性。
利益冲突申明 本研究无任何利益冲突
作者贡献声明 向圣锦:参与酝酿和实验设计, 收集数据, 资料的分析和解释; 撰写论文; 根据编辑部的修改意见进行修改。李童:参与课题设计和负责实验的实施, 分析解释数据, 统计分析, 文章审阅修改。姜小涵:负责部分实验的具体实施, 分析解释数据, 统计分析, 文章审阅修改。池在龙:负责课题的选题、设计, 资料的分析和解释, 修改论文中关键性结果、结论, 根据编辑部的修改意见进行核修
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|