第一作者:曹琼洁(ORCID:0000-0002-6890-9603),Email:vicky.cqj@163.com
目的 研究microRNA-127(miR-127)在人葡萄膜黑色素瘤细胞中的表达水平及其对细胞增殖的影响。方法 实验研究。通过实时荧光定量PCR(RT-qPCR)法检测miR-127在葡萄膜黑色素瘤细胞M23和SP6.5与正常葡萄膜黑色素细胞UM95中的表达水平。细胞实验通过阳离子脂质体介导的方法将miR-127和阴性对照(NC)转染入M23和SP6.5中,并应用细胞增殖实验法(MTS法)和流式细胞技术分别检测细胞增殖能力和细胞周期,采用Western Blot法检测转染miR-127后细胞周期相关蛋白的表达。另外,通过RT-qPCR检测用表观药物5-氮杂-2-脱氧胞苷(5-Aza-dC)和(或)曲古抑菌素A(TSA)处理后的M23和SP6.5细胞内miR-127的表达水平。MiR-127的表达量及细胞实验各参数在2组间比较采用独立样本 t检验。结果 miR-127在M23和SP6.5中的表达水平低于UM95( t=72.2、591.5, P<0.001)。MTS结果显示,在M23和SP6.5细胞中,转染miR-127组相对细胞数目较NC组的100%分别减少至(62.3±4.2)%和(65.4±2.3)%,差异具有统计学意义( t=12.7、21.6, P<0.001)。流式细胞技术分析显示,转染miR-127组处于G0/G1期的M23和SP6.5细胞数量比例明显高于NC组( t=-6.7, P=0.003; t=-9.9, P<0.001),同时处于S期的M23和SP6.5细胞数量比例明显低于NC组( t=8.6, P=0.001; t=12.7, P<0.001)。Western Blot结果表明miR-127可明显降低M23和SP6.5细胞内磷酸化Rb蛋白的表达水平( t=22.2、15.6, P<0.001)。此外,miR-127在M23和SP6.5细胞中的表达可被5-Aza-dC和TSA诱导上调( P<0.05)。结论 miR-127通过抑制细胞周期而抑制人葡萄膜黑色素瘤细胞的增殖,并可被DNA甲基化和组蛋白乙酰化表观遗传机制调控。
Objective: We investigated the expression and regulation of microRNA-127 (miR-127) in uveal melanoma cells. We also investigated the effect of epigenetically upregulating miR-127 by altering DNA methylation and histone acetylation.Methods: In this experimental study, we performed real-time reverse transcriptase quantitative polymerase chain reaction (RT-qPCR) to detect the expression level of miR-127 in both uveal melanoma cells (M23 and SP6.5) and uveal melanocytes (UM95). Lipofectamine RNAiMAX reagent was used to transfect M23 and SP6.5 with either miR-127 or a negative control (NC). The proliferation of uveal melanoma cells was quantified by 3-[4, 5-dimethyl-thiazol-2-yl]-5-[3-carboxymethoxyphenyl]-2-[4-sulfophenyl]-2H-tetrazo-lium, inner salt (MTS) cell proliferation assay. Cell cycle was examined by flow cytometry. The expression of cell cycle-related proteins was analyzed by Western Blot. In addition, RT-qPCR was performed to detect the expression level of miR-127 in M23 and SP6.5 cells after treatment with 5-aza-2-deoxycytidine (5-Aza-dC) and trichostatin A (TSA). These agents modify gene expression through DNA methylation and histone acetylation, respectively. Data were analyzed using independent t-tests.Results: miR-127 was dramatically downregulated in M23 and SP6.5 cells as compared to UM95 ( t=72.2, 591.5, P<0.001). The MTS assay showed that the relative number of cells transfected with miR-127 [(62.3±4.2)% and (65.4±2.3)%] was significantly lower than transfected with NC ( t=12.7, 21.6, P<0.001). Flow cytometry showed that the percentage of M23 and SP6.5 cells transfected with miR-127 in G0/G1 phase was significantly higher than for the NC group ( t=-6.7, P=0.003; t=-9.9, P<0.001), and the percentage of M23 and SP6.5 cells in the S phase was significantly lower than for the NC group ( t=8.6, P=0.001; t=12.7, P<0.001). Furthermore, miR-127 downregulated the level of phosphorylated retinoblastoma protein in uveal melanoma cells. In addition, miR-127 was upregulated after treatment with 5-Aza-dC and/or TSA ( P<0.05).Conclusions: Our results demonstrated that miR-127 can suppress uveal melanoma cell proliferation by inhibition of cell cycle. Furthermore miR-127 expression was modulated by epigenetic regulation including DNA methylation and histone acetylation.
MicroRNA(miRNA)是一类长约22个核苷酸的内源性非编码RNA, 参与调节个体发育、免疫保护、肿瘤发生等许多生理和病理过程[1, 2]。miRNA通过与RNA诱导沉默复合体(RNA-induced silencing complex, RISC)相结合, 然后靶向特定的mRNA而使之降解或抑制其翻译[3]。有研究表明, miRNA与癌症的发生具有密切联系, 50%以上已知miRNA位于肿瘤相关的基因脆性位点, 其在不同类型的肿瘤中, 起着致癌因子或抑癌因子的双重作用[4]。
葡萄膜黑色素瘤是成人中最常见的原发性眼内恶性肿瘤, 占黑色素瘤的5%~6%[5]。葡萄膜黑色素瘤恶性程度高, 易随血行转移, 缺乏淋巴引流, 临床上超过50%的患者会出现转移, 并且转移后的生存率非常低[6]。越来越多的研究发现, 许多miRNA在高转移风险的葡萄膜黑色素瘤细胞中表达降低, 并且对葡萄膜黑色素瘤细胞的生长具有明显的调控作用, 如miR-34a、miR-137和miR-124a在葡萄膜黑色素瘤组织或细胞中显著下调, 并通过调节靶基因表达抑制葡萄膜黑色素瘤细胞的生长与迁移[7, 8, 9]。而miR-127对人眼葡萄膜黑色素瘤细胞的生长是否具有调控作用尚不清楚。
本研究通过实时荧光定量PCR(RT-qPCR)检测miR-127在人葡萄膜黑色素瘤细胞与正常葡萄膜黑色素细胞中的表达量, 然后在细胞中过表达miR-127来研究其对细胞增殖、细胞周期的影响。此外, 本研究还揭示了表观药物5-氮杂-2-脱氧胞苷(5-Aza-dC)和曲古抑菌素A(TSA)对miR-127的调控作用, 为临床上葡萄膜黑色素瘤的治疗提供了新的思路。
人眼葡萄膜黑色素细胞UM95和人眼葡萄膜黑色素瘤细胞M23由美国纽约大学附属眼耳医院胡诞宁教授惠赠; 人眼葡萄膜黑色素瘤细胞SP6.5由加拿大魁北克免疫学研究中心惠赠。
Dulbecco's Modified Eagle Medium(DMEM)培养基、Trypsin-EDTA(0.05%)、胎牛血清(Fetal bovine serum, FBS)、Lipo-fectamineTM RNAi MAX转染试剂、Trizol、RIPA裂解液均购自美国Invitrogen公司, miR-127和随机序列寡核苷酸链均购自美国Ambion公司, RT-qPCR所用试剂和探针均购自美国ABI公司, Cycletest Plus DNA Reagent试剂盒购于美国BD公司, 磷酸化Rb蛋白(p-Rb)抗体购自美国Cell Signaling Technology公司, 硝酸纤维素膜购于德国GE Healthcare公司, 细胞增殖实验(MTS法)试剂盒购自美国Promega公司, 5-Aza-dC和TSA购自美国Sigma公司, 7500型荧光实时定量PCR仪和SpectraMax M5酶标仪购自美国Molecular Devices公司。
1.3.1 细胞培养 UM95和M23、SP6.5细胞均培养于含10% FBS的DMEM培养基, 置于37 ℃、含5% CO2的培养箱中, 采用0.05%胰蛋白酶消化传代。
1.3.2 细胞RNA提取及实时荧光定量PCR Trizol试剂法分别提取UM95、M23和SP6.5细胞的总RNA, 采用Taq Man Micro RNA Assays试剂盒, 针对miR-127逆转录合成cDNA, 再用探针法检测各细胞中miR-127的表达水平, 以U6为内参, 用2-△ △ Ct法分析目的基因相对表达量。所有PCR操作定量均在7500型荧光实时定量PCR仪按标准体系标准程序完成。
1.3.3 脂质体转染 将M23和SP6.5细胞接种于多孔培养板, 随机分为实验组和对照组。采用LipofectamineTM RNAi/MAX转染试剂将miR-127转染入实验组细胞(终浓度50 nmol/L), 以相同方法将一段长度和结构都与miRNA类似的随机序列寡核苷酸链作为阴性对照(Negative control, NC)转染入对照组细胞, 方法参考文献[10]。
1.3.4 细胞增殖实验 对数生长期的M23和SP6.5细胞以3× 103/孔均匀接种到96孔板中, 每组设6个复孔。细胞培养24 h后按上述方法转染miR-127或NC, 转染5 d后进行MTS检测, 即弃去培养基, 于每孔中加入80 μ l无血清F12培养液和20 μ l MTS混合液(MTS∶ PMS=19∶ 1), 37 ℃孵育2 h后, 用酶标仪在490 nm波长下读取光密度值(OD)。计算相对细胞数目=实验组OD值/对照组OD值× 100%。
1.3.5 流式细胞术检测细胞周期 M23和SP6.5细胞转染miR-127或NC, 方法同上。转染48 h后用0.05%胰蛋白酶消化细胞并收集细胞, 经70%乙醇固定和碘化丙啶(Propidium iodide, PI)染色后, 进行流式细胞术检测, 每个样本收集30 000个细胞, 通过Modifit软件计算细胞周期各时相的百分率。
1.3.6 Western Blot实验 M23和SP6.5细胞转染miR-127或NC, 方法同上。48 h后用RIPA裂解液裂解细胞, 提取实验组及对照组细胞的总蛋白。蛋白经SDS聚丙烯酰胺凝胶电泳分离后转移至硝酸纤维素膜上, 经5%脱脂奶粉-PBST封闭液封闭3 h后, 用稀释比例为1∶ 800的一抗p-Rb于4 ℃孵育过夜, 经PBS洗脱后再用1∶ 5 000的带有荧光基团标记的二抗在室温孵育2 h, 最后在Odyssey Licor双色红外激光成像仪上进行曝光成像。Western Blot结果通过Image pro plus软件计算灰度值, 目的蛋白的表达量=目的蛋白的灰度值/内参GAPDH的灰度值。
1.3.7 表观药物处理 5-Aza-dC及TSA使用DMSO分别溶解成1 mg/ml的贮存液, 临用时使用完全培养基稀释成所需的工作浓度。对数生长期的M23和SP6.5细胞以1× 105/孔均匀接种到24孔板中, 分成以下6组[11]:①对照组:完全培养基培养(加入与实验组等量的DMSO)48 h; ②1 μ mol/L 5-Aza-dC组含5-Aza-dC终浓度为1 μ mol/L的培养基培养48 h; ③5 μ mol/L 5-Aza-dC组含5-Aza-dC终浓度为5 μ mol/L的培养基培养48 h; ④TSA组:含TSA终浓度为100 ng/ml的培养基培养16 h; ⑤1 μ mol/L 5-Aza-dC+TSA组在5-Aza-dC为1 μ mol/L的培养基中培养32 h后加入TSA 100 ng/ml培养16 h; ⑥5 μ mol/L 5-Aza-dC+TSA组:在5-Aza-dC浓度为5 μ mol/L的培养基中培养32 h后再加TSA 100 ng/ml培养16 h。48 h后, Trizol裂解细胞, 提取细胞总RNA, RT-qPCR法检测miR-127表达水平。
实验研究。数据采用SPSS 16.0软件进行统计学分析。实验均重复3次, 数据以$\bar{x}\pm s$表示, 两两比较采用独立样本t检验。以P< 0.05为差异有统计学意义。
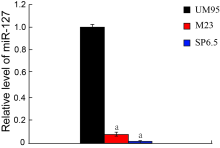
miR-127在葡萄膜黑色素瘤细胞M23和SP6.5中的表达量明显低于原代培养的葡萄膜黑色素细胞UM95。与UM95细胞比较, miR-127在M23细胞中降低了91.8%± 2.1%(t=72.2, P< 0.001), 在SP6.5细胞中降低了99.2%± 0.1%(t=591.5, P< 0.001), 差异均有统计学意义。见图1。
转染5 d后, 在M23细胞中, miR-127组相对细胞数目为(62.3± 4.2)%, 与NC组(100%)相比明显减少, 差异具有统计学意义(t=12.7, P< 0.001); 在SP6.5细胞中, miR-127组相对细胞数目为(65.4± 2.3)%, 与NC组(100%)相比明显下降, 差异具有统计学意义(t=21.6, P< 0.001)。
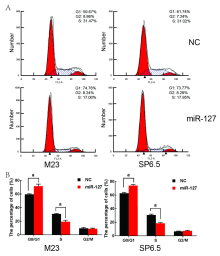
miR-127组M23细胞处于G0/G1期细胞数量比例为(71.6± 3.0)%, 显著高于NC组的(59.6± 0.7)%, S期细胞比例为(19.3± 2.2)%, 显著低于NC组的(30.8± 0.8)%, 差异均有统计学意义(t=-6.7, P=0.003; t=8.6, P=0.001)。2组间G2/M期细胞数量差异无统计学意义(t=0.6, P=0.60); miR-127组SP6.5细胞处于G0/G1期细胞数量比例为(74.0± 1.4)%, 显著高于NC组的(62.7± 1.5)%, S期细胞比例为(18.5± 1.1)%, 显著低于NC组的(30.7± 1.2)%, 差异均有统计学意义(t=-9.9, P< 0.001; t=12.7, P< 0.001), 2组间G2/M期细胞数量差异无统计学意义(t=-1.5, P=0.21), 见图2。这说明miR-127能够诱导葡萄膜黑色素瘤细胞阻滞在G1期, 无法顺利向S期过渡。
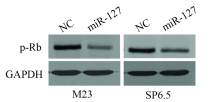
miR-127组M23细胞中磷酸化Rb蛋白p-Rb的表达量为0.3± 0.1, 与NC组的1.5± 0.1相比明显下降, 差异有统计学意义(t=22.2, P< 0.001); miR-127组SP6.5细胞中p-Rb的表达量为0.3± 0.1, 与NC组的1.0± 0.1相比也明显下降, 差异有统计学意义(t=15.6, P< 0.001)。见图3。
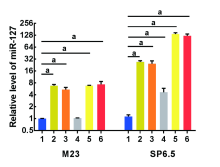
2.5 5-Aza-dC和TSA对葡萄膜黑色素瘤细胞中miR-127的表达影响
与对照组相比, 经5-Aza-dC单独或和TSA联合干预后的M23细胞中miR-127的表达量均有明显升高, 升高倍数分别为6.7± 0.5、5.4± 0.7、6.8± 0.2、7.3± 1.3, 差异有统计学意义(t=20.0, P< 0.001; t=10.7, P< 0.001; t=63.2, P< 0.001; t=8.3, P=0.001); 此外, 经2种浓度5-Aza-dC处理的SP6.5中miR-127的相对表达水平也大幅度升高, 升高倍数分别为27.0± 2.0、24.4± 4.4, 差异有统计学意义(t=21.9、9.2, 均P< 0.001), 2种药物药联合处理后表达量升高更为显著, 升高倍数分别为136.8± 11.3、123.9± 13.7, 差异有统计学意义(t=20.8、15.5, 均P< 0.001)。TSA单独干预后SP6.5细胞中miR-127的表达量明显升高了(4.6± 1.2)倍(t=5.0, P=0.007), 而M23细胞中miR-127的表达量无明显变化, 差异不具有统计学意义(t=2.5, P=0.07)。见图4。
在1973年至2008年期间, 人群中葡萄膜恶性黑色素瘤的发病率为1/106[12]。虽然目前的治疗手段有了明显提升, 但是大多数患者会经历失明, 超过三分之一的患者需要通过手术摘除眼球[13], 并且术后仍有40%~50%的患者会发生转移, 发生肝转移患者的生存率非常低, 存活时间几乎不到1年[14]。而手术作为治疗葡萄膜黑色素瘤的最有效方法之一, 主要还是基于局部控制治疗, 却无针对性的个性化治疗, 预后差。
miRNA是当前肿瘤学领域的研究热点之一, 在葡萄膜黑色素瘤的发生发展中起重要作用。miR-34a通过下调c-Met表达, 抑制葡萄膜黑色素瘤细胞的增殖和迁移能力[7]。miR-137则通过负调节MITF, 导致葡萄膜黑色素瘤细胞阻滞在G1期, 抑制细胞生长[8]。miR-182也可以通过下调靶基因MITF、BCL2和cyclin D2等抑制细胞的生长、迁移, 并促进凋亡[15]。
本研究通过实时定量PCR发现在人眼葡萄膜黑色素瘤细胞系中, miR-127水平显著下调, 这提示miR-127在葡萄膜黑色素瘤发生过程中也可能起到重要的调控作用。已有不少研究发现miR-127可能参与多种肿瘤的发生过程, wang等[16]发现miR-127-3p可以通过靶向调节ITGA6来抑制骨肉瘤细胞的增殖、迁移和侵袭, 并促进细胞凋亡。Shi等[17]研究表明miR-127与肺腺癌的发生和不良预后有关。此外, miR-127-5p在人肝癌细胞中通过直接靶向BLVRB抑制NF-κ B活性, 或者通过其他靶基因如Sept7、HMGB2等, 对细胞增殖迁移起负调控作用[18, 19, 20]。本研究通过在M23和SP6.5细胞中转染使其过表达发现miR-127能明显抑制细胞增殖, 同时流式细胞术结果进一步表明miR-127导致M23和SP6.5细胞阻滞在G1期, 由于G1期是细胞周期中DNA合成的能量和物质准备阶段, G1期的长短在很大程度上决定了细胞周期的长短, 即细胞增殖的速度。Rb蛋白在细胞周期中最为关键的调控点G1/S起到一种“ 闸门” 的作用, Rb蛋白通过与转录因子E2F结合, 抑制细胞从G1期进入S期, 磷酸化修饰则使Rb蛋白与E2F解离, 促使细胞从G1期进入S期。在转染了miR-127后M23和SP6.5细胞中的p-Rb发生显著下调, 说明miR-127可通过调控细胞周期相关蛋白p-Rb使葡萄膜黑色素瘤细胞在G1期出现明显的滞留, 使其无法顺利向S期过渡, 从而抑制细胞增殖。5-Aza-dC目前已被美国食品药品管理局批准作为第一个在临床上用于治疗恶性肿瘤的DNA去甲基化药物, 可以使发生DNA高甲基化的抑癌基因再次活化[21]。TSA则是一种广谱的组蛋白去乙酰化酶抑制剂, 能够提高组蛋白乙酰化水平, 目前广泛用于表观遗传研究领域[22, 23]。本研究发现经5-Aza-dC单独或和TSA联合干预后的细胞中miR-127表达水平显著升高, 且联合用药组升高更明显, 表明2种药联用具有协同作用, 这可能与DNA去甲基化通过甲基结合蛋白和组蛋白去乙酰化酶相互作用有关[24]。
综上所述, miR-127在葡萄膜黑色素瘤细胞中显著下调, 并可作为表观药物5-Aza-dC以及TSA的作用靶点, 通过抑制细胞周期而显著抑制葡萄膜黑色素瘤细胞的增殖, 本研究为葡萄膜黑色素瘤的临床诊断和治疗提供了新的思路, 具有十分重要的理论价值和应用前景。
利益冲突申明 本研究无任何利益冲突
作者贡献声明 曹琼洁:参与选题设计, 实验研究, 收集数据, 资料的分析和解释; 撰写论文; 根据编辑部的修改意见进行修改。董菁、李丽:参与实验研究, 收集数据, 资料的分析和解释。陈晓燕、王教:参与选题、设计和修改论文的结果、结论。闫东升:参与选题、设计、资料的分析和解释, 修改论文中关键性结果、结论, 根据编辑部的修改意见进行核修
The authors have declared that no competing interests exist.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|